
2026年3月24日,达安集团赛隽生物自主研发的异体人骨髓间充质干细胞注射液(管线代号:CG-BM1)已正式获得临床试验默示许可,适应症为绝经后骨质疏松症(PMOP)。
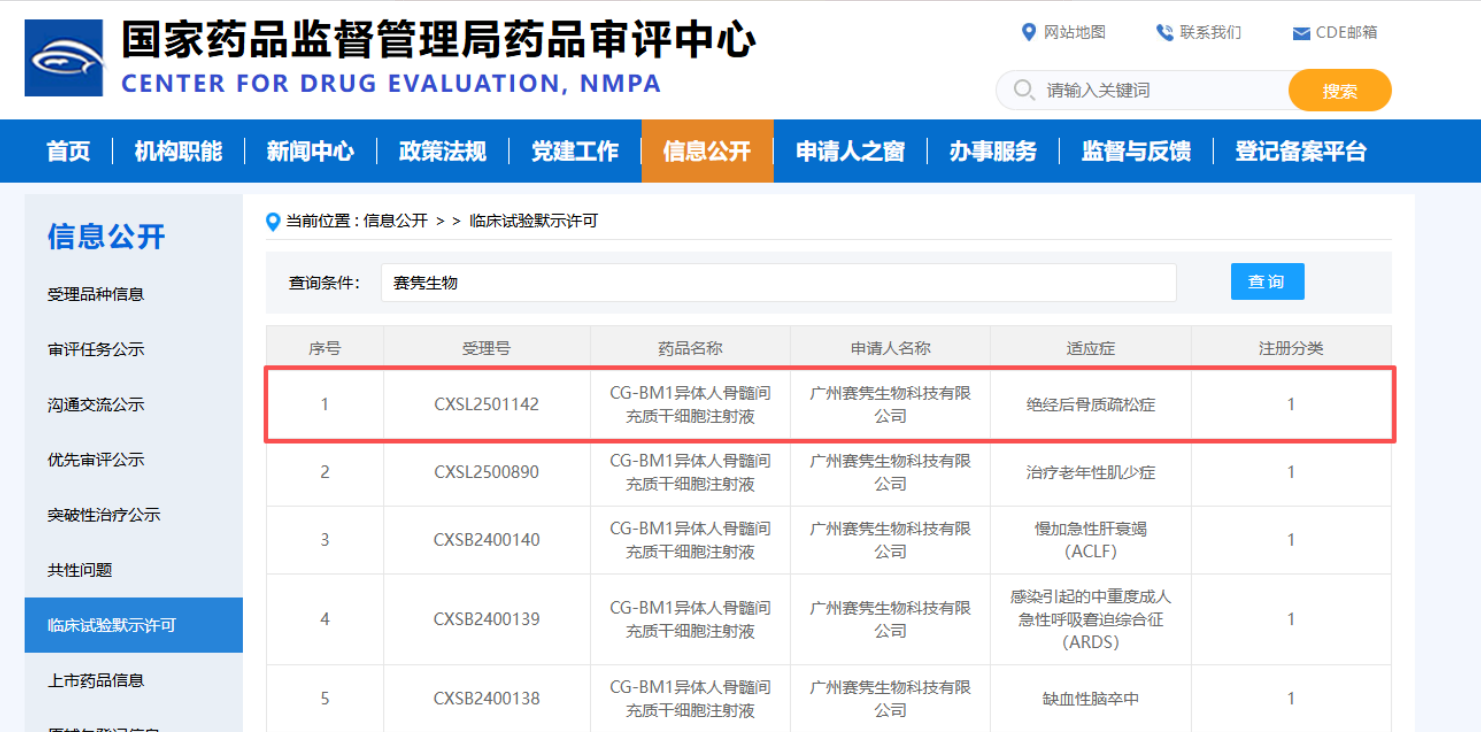
根据Insights数据库,CG-BM1是全球首个获得新药临床试验申请(IND)批准的用于治疗绝经后骨质疏松症的骨髓间充质干细胞(MSC)药物。作为专注细胞治疗与再生医学的创新生物医药公司,达安集团赛隽生物已于2026年1月获批针对老年性肌少症的IND,此次新获批的适应症是
该公司在退行性疾病领域取得的又一重要里程碑,也是公司累计的干细胞第五项IND!
作为国内领先的细胞治疗及再生医学创新生物医药企业,达安集团赛隽生物此次CG-BM1治疗绝经后骨质疏松适应症IND的获批,与今年获批的“老年性肌少症”IND(全球首个进入临床阶段的相关干细胞药物)形成了高度的战略协同。这意味着达安集团赛隽生物已在老龄化相关的重大退行性疾病领域构筑了高度差异化的管线矩阵,有效规避常规适应症的同质化竞争,展现出对前沿临床价值的敏锐洞察。
凭借“药品监管+生物医学新技术”双轨驱动模式,达安集团赛隽生物已经成功奠定了产业布局和商业化落地方面的先发优势。未来,赛隽生物将联合达安生命细胞库,打通“细胞存储+细胞治疗”的闭环,有望满足更多未被满足的临床需求,为患者带来新的治疗选择,并助力我国细胞治疗从“跟跑”、“并跑”迈向全球“领跑”。